 林双君
林双君
研究员
微生物次代谢物的生物合成
Email: linsj@sjtu.edu.cn
林双君,男,博士,研究员,博士生导师。2002年于中国科学院化学研究所获博士学位后,先后在加拿大埃尔伯塔大学和美国威斯康星大学麦迪逊分校从事博士后和研究助理工作,现任上海交通大学生命科学技术学院,微生物代谢国家重点实验室研究员。
1996年毕业于吉林大学化学系,获理学学士学位。1999年毕业于中国科学院上海药物研究所获有机化学硕士学位。2002年于中国科学院化学研究所获有机化学博士学位。2002-2005年在加拿大埃尔伯塔大学化学系(University of Alberta)从事博士后研究,主要从事糖基转移酶的功能研究及其在寡糖生物合成中的应用。2005-2008年在美国威斯康星大学麦迪逊分校(University of Wisconsin-Madison)从事微生物次代谢物的生物合成研究。于2008年10月回国加入上海交通大学生命科学技术学院,特别研究员,博士生导师。迄今,在 JACS, PNAS, Nature Structural & Molecular Biology, J. Org. Chem., 和J. Biol. Chem.等国际期刊发表研究论文50余篇。
研究领域: 具有显著生理活性的微生物源天然产物的化学生物学
1. 生物活性天然产物的发现及结构鉴定,天然产物的生物合成及合成生物学。微生物特别是链霉菌,是临床应用抗生素的重要来源。以特殊环境来源的放线菌作为源泉,筛选和分离纯化具有抗菌、抗肿瘤活性的天然产物。
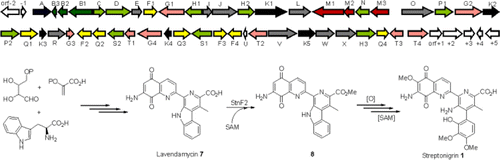
Fig 1 Characterization of Streptonigrin Biosynthesis Reveals a Cryptic Carboxyl Methylation and an Unusual Oxidative Cleavage of a N-C Bond (Wu, et al. J Am Chem Soc, 2013)
2. 天然产物的生物合成与组合生物合成,具有重要生理活性的微生物次级代谢产物的挖掘。课题组主要以微生物源生物碱类天然产物(如抗肿瘤生物碱链黑霉素、莱沃德霉素、稀疏菌素,及海洋霉素和FR 900452)及非核糖体肽类细胞凋亡诱导剂Chloptosin和Polyoxypeptin为研究目标,确定这些天然产物的生物合成基因簇,阐明其生物合成途径,揭示途径中新颖酶催化反应的分子机制。然后运用生物合成技术、组合生物合成技术及合成生物学技术,构建新的合成途径,创制新的“人工“天然产物。
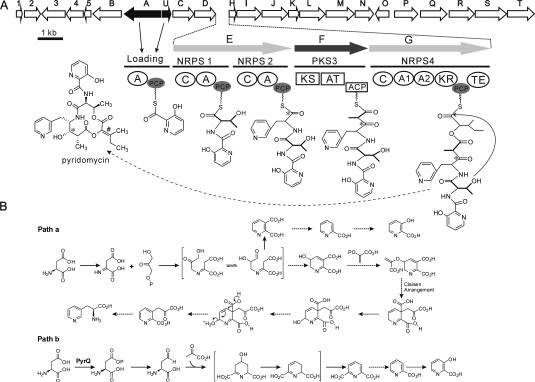
Fig 2 Organization of the pyridomycin biosynthetic gene cluster and model for the biosynthesis of pyridomycin. (Huang, et al. J Biol Chem. 2011)
3.酶催化反应的机理和应用。生物催化剂具有其独特的催化性能如优秀的化学选择性,区域选择性和立体选择性,因此生物催化剂是一种具有广泛应用前景的有机合成催化工具。通过对酶的催化机理的阐明,拓展酶在有机合成特别是药物中间体和精细化学品合成方面的应用。

Fig 3 A Trans-acting Ketoreductase in Biosynthesis of a Symmetric Polyketide Dimer SIA7248 (Zou, et al. Chembiochem. 2013)
教育经历
1992年-1996年 吉林大学化学系,本科/理学学士
1996年-1999年 中国科学院上海药物研究所,研究生/理学硕士
1999年-2002年 中国科学院化学研究所,研究生/理学博士
1996年-1999年 中国科学院上海药物研究所,研究生/理学硕士
1999年-2002年 中国科学院化学研究所,研究生/理学博士
工作经历
2002年-2005年 加拿大埃尔伯塔大学化学系,博士后。主要从事糖基转移酶的生物学功能及在寡糖生物合成的应用研究。
2005年-2008年 美国威斯康星大学麦迪逊分校药学院,研究助理。主要从事微生物次级代谢产物烯二炔类抗生素的生物合成机制及酶学功能研究。
2008年11月-至今 上海交通大学生命科学技术学院,微生物代谢国家重点实验室,研究员,博士生导师荣誉奖励
2011年入选教育部“新世纪优秀人才支持计划”
2012年入选上海交通大学晨星奖励计划“A”类
发表论文
1. Kong D, Lee MJ, Lin S*, Kim ES*. Biosynthesis and Pathway Engineering of Antifungal Polyene Macrolides in Actinomycetes. J Ind Microbiol Biotechnol. 2013 Mar 21. [Epub ahead of print].
2. Lin S, Huang T, Shen B*. Tailoring enzymes acting on carrier protein-tethered substrates in natural product biosynthesis. Methods Enzymol. 2012, 516, 321-43.
3. Lin S, Huang T, Horsman GP, Huang SX, Guo X, Shen B*. Specificity of the ester bond forming condensation enzyme SgcC5 in C-1027 biosynthesis. Org Lett. 2012, 14, 2300-3.
4. Huang T, Wang Y, Yin J, Du Y, Tao M, Xu J, Chen W, Lin S*, Deng Z. Identification and characterization of the pyridomycin biosynthetic gene cluster of Streptomyces pyridomyceticus NRRL B-2517. J Biol Chem. 2011, 286, 20648-57.
5. Lin S, Horsman GP, Shen B*. Characterization of the epoxide hydrolase NcsF2 from the neocarzinostatin biosynthetic gene cluster. Org Lett. 2010, 12, 3816-9.
6. Lin S, Horsman GP, Chen Y, Li W, Shen B*. Characterization of the SgcF epoxide hydrolase supporting an (R)-vicinal diol intermediate for enediyne antitumor antibiotic C-1027 biosynthesis. J Am Chem Soc. 2009,131, 16410-7. 7.
7. Lin S, van Lanen SG, Shen B*. A free-standing condensation enzyme catalyzing ester bond Formation in C-1027 Biosynthesis. PNAS 2009, 106,4183-8.
8. Lin S, Van Lanen SG and Shen B*. “Regiospecific Chlorination of (S)-b-Tyrosyl-S -Carrier Protein Catalyzed by SgcC3 in the Biosynthesis of the Enediyne Antitumor Antibiotic C-1027”. J. Am. Chem. Soc.2007, 129, 12432-8.
9. Lin S,Van Lanen SG and Shen B*. “Characterization of the Two-Component, FAD- Dependent Monooxygenase SgcC that Requires Carrier Protein-Tethered Substrates for the Biosynthesis of the Enediyne Antitumor Antibiotic C-1027”. J. Am. Chem. Soc.2008, 130, 6616-6623.
2. Lin S, Huang T, Shen B*. Tailoring enzymes acting on carrier protein-tethered substrates in natural product biosynthesis. Methods Enzymol. 2012, 516, 321-43.
3. Lin S, Huang T, Horsman GP, Huang SX, Guo X, Shen B*. Specificity of the ester bond forming condensation enzyme SgcC5 in C-1027 biosynthesis. Org Lett. 2012, 14, 2300-3.
4. Huang T, Wang Y, Yin J, Du Y, Tao M, Xu J, Chen W, Lin S*, Deng Z. Identification and characterization of the pyridomycin biosynthetic gene cluster of Streptomyces pyridomyceticus NRRL B-2517. J Biol Chem. 2011, 286, 20648-57.
5. Lin S, Horsman GP, Shen B*. Characterization of the epoxide hydrolase NcsF2 from the neocarzinostatin biosynthetic gene cluster. Org Lett. 2010, 12, 3816-9.
6. Lin S, Horsman GP, Chen Y, Li W, Shen B*. Characterization of the SgcF epoxide hydrolase supporting an (R)-vicinal diol intermediate for enediyne antitumor antibiotic C-1027 biosynthesis. J Am Chem Soc. 2009,131, 16410-7. 7.
7. Lin S, van Lanen SG, Shen B*. A free-standing condensation enzyme catalyzing ester bond Formation in C-1027 Biosynthesis. PNAS 2009, 106,4183-8.
8. Lin S, Van Lanen SG and Shen B*. “Regiospecific Chlorination of (S)-b-Tyrosyl-S -Carrier Protein Catalyzed by SgcC3 in the Biosynthesis of the Enediyne Antitumor Antibiotic C-1027”. J. Am. Chem. Soc.2007, 129, 12432-8.
9. Lin S,Van Lanen SG and Shen B*. “Characterization of the Two-Component, FAD- Dependent Monooxygenase SgcC that Requires Carrier Protein-Tethered Substrates for the Biosynthesis of the Enediyne Antitumor Antibiotic C-1027”. J. Am. Chem. Soc.2008, 130, 6616-6623.
10. Van Lanen SG, Lin S and Shen B*. “The Biosynthesis of the Enediyne Antitumor Antibiotic C-1027 Involves a New Branching Point in Chorismate Metabolism” PNAS. 2008, 105, 494-499.
11. Luo YG, Lin S, Zhang J. Cooke HA, Bruner SD, and Shen B. “Regiospecific O- methylation of naphthoic acids catalyzed by NcsB1, an O-methyltransferase involved in the biosynthesis of the enediyne antitumor antibiotic neocarzinostatin” J. Biol. Chem. 2008, 283, 14694-14702
12. Greco A, Ho JGS, Lin SJ, Palcic MM, Rupnik M, Ng KKS, “Carbohydrate recognition by Clostridium difficile toxin A” Nature Structural & Molecular Biology 2006, 13, 460-1.
13. Wang MX*, Lin SJ, Liu J, et al. “Efficient biocatalytic synthesis of highly enantiopure alpha-alkylated arylglycines and amides” Advanced Synthesis & Catalysis. 2004,346, 439-45.
14. Wang MX*, Lin SJ, Liu CS, et al. “Nitrile biotransformations for highly efficient and enantioselective syntheses of electrophilic oxiranecarboxamides” J. Org. Chem. 2003, 68, 4570-3.
15. Wang MX*, Lin SJ. “Practical and convenient enzymatic synthesis of enantiopure alpha-amino acids and amides” J. Org. Chem. 2002, 67, 6542-5.
16. Lin SJ, Jiang SH, Zhu DY*, et al. “Two novel iridoids from Scrophularia buergeriana” . Tetrahedron Lett. 2000, 41, 1069-71.
Copyright © 2016上海交通大学分子微生物学研究室
地址:上海市华山路1954号上海交通大学哲生馆(原科学馆) 电话:021-62932943
